
静岡発のバイオスタートアップががん再発検査技術を開発へ
静岡発のバイオスタートアップががん再発検査技術を開発へ
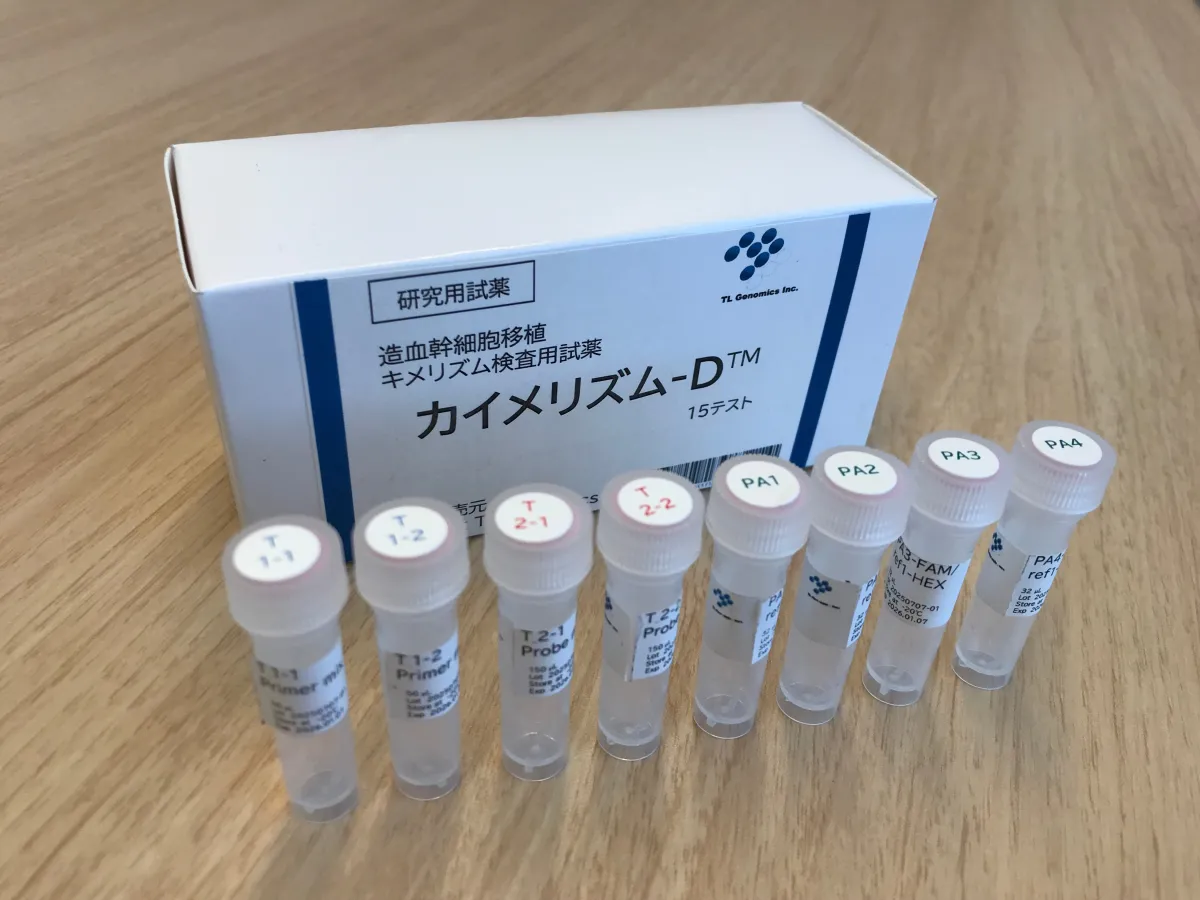
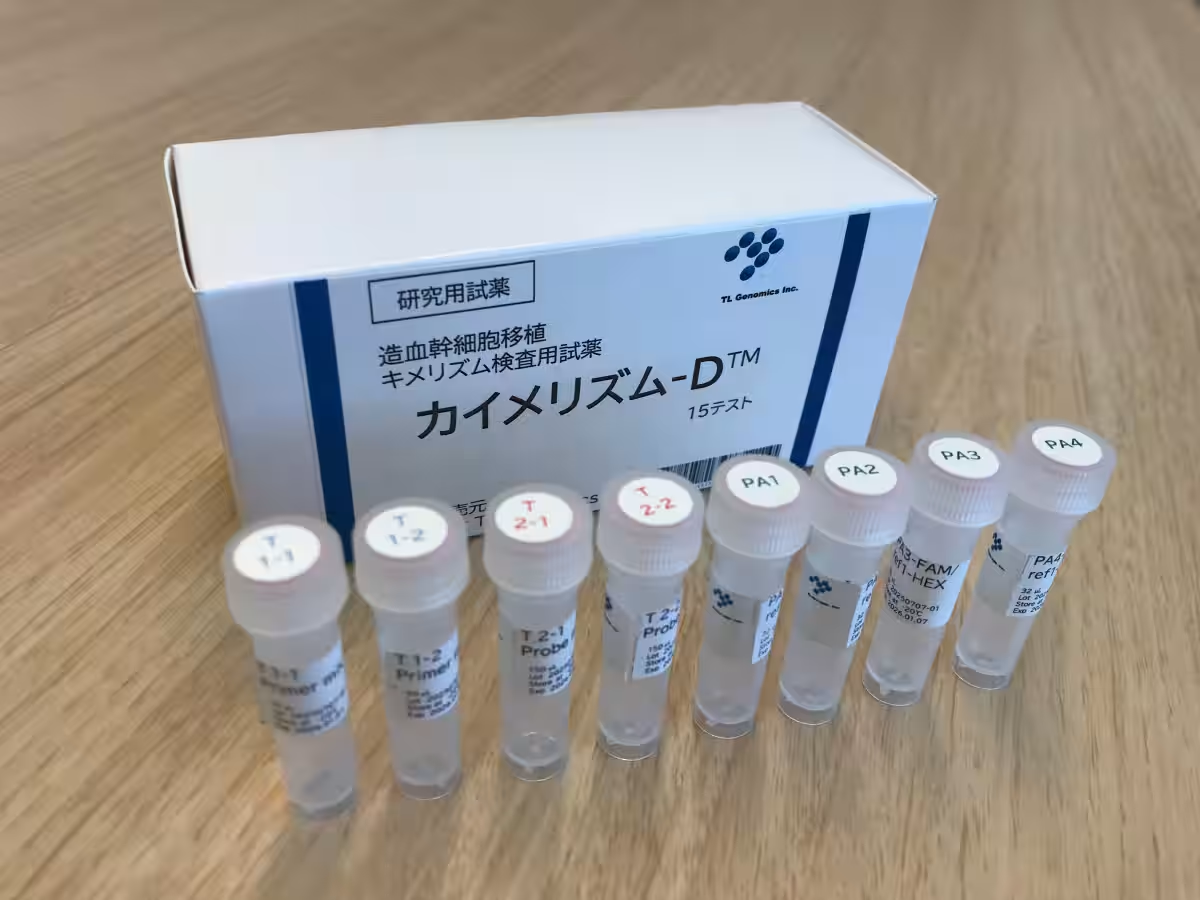
静岡県三島市に本拠を置く株式会社TL Genomicsは、地域のスタートアップ支援制度を利用し、資金調達に成功しました。ファンド支援を受けることで、骨髄移植後のがん再発をモニタリングするための新しいDNA検査「キメリズム検査」の承認を進めています。
背景:年間3,500人が直面する再発の不安
骨髄移植による治療は血液がん治療の重要な手段ですが、患者には移植後の「再発」の不安が常につきまといます。日本では年間約3,500件の骨髄移植が行われており、患者は再発を早期に検出するための新たな検査が必要とされています。しかし、現在の保険適用検査には様々な制約があり、患者の心理的負担を軽減できていません。
既存の検査の問題点
現在利用可能な検査には大きな問題が2つあります。まず、既存の「異性間FISH法」は性別が異なるドナーと患者にしか使えず、同性間の移植では無力です。また、この方法は再発の経過観察には適していないため、医療現場での実用性が低いと言わざるを得ません。
次に、保険適用外の「STR-PCR法」は高額な検査費用がかかり、しかも感度が低いため初期のがん細胞を見逃すリスクがあります。このような現状を受け、TL Genomicsは新しい技術の開発に取り組んでいます。
新技術「InDel-dPCR法」の優位性
大阪大学との共同研究により、TL GenomicsはデジタルPCR技術と個人識別DNA「InDelマーカー」を使用した「InDel-dPCR法」を開発しました。この新技術には3つの大きな優位性があります。
1. 検出感度の向上
従来の検査法に比べ、検出感度が約10倍向上しています。これにより、微量ながん細胞も早期に発見することが可能になります。これが患者の治療戦略に大きく寄与することでしょう。
2. コストダウン
既存の同様の技術が高額である一方、TL Genomicsは検査コストを1/20にまで削減することを目指しています。例えば、タイピング用の検査は25,000円、モニタリング用は15,000円を見込んでいます。
3. 幅広い適用範囲
同性・異性を問わず、全ての患者に対応できる検査法は、従来の検査法によって訴えられていた制約を克服しています。これにより、より多くの人が安心して検査を受けることができるようになります。
未来への展望
また、今回の資金調達は静岡県の「ファンドサポート事業」によるもので、静岡県内での製造拠点設立が予定されています。代表の久保知大氏は、地域に根付いたビジネスを目指し、静岡SHIPやがんセンターとの連携を進めています。2026年には承認申請を行い、2028年には市場を開放する予定です。
医療のスタンダードを目指して
この技術が実用化されれば、再発検査の新しいスタンダードが日本に導入され、血液がん患者の不安が大きく軽減されると期待されています。TL Genomicsは、今後も新たな医療のスタンダードを作り上げるため、地域社会とともに進展を続けていくでしょう。今後の彼らの活躍に注目です。




関連リンク
サードペディア百科事典: 静岡県 TL Genomics がん再発検査
トピックス(その他)









【記事の利用について】
タイトルと記事文章は、記事のあるページにリンクを張っていただければ、無料で利用できます。
※画像は、利用できませんのでご注意ください。
【リンクついて】
リンクフリーです。